METABOLINK
Cédric Dray
Armelle Yart
Interactions métaboliques et perte de fonctions liées à l’âge, résilience métabolique face à la fragilité
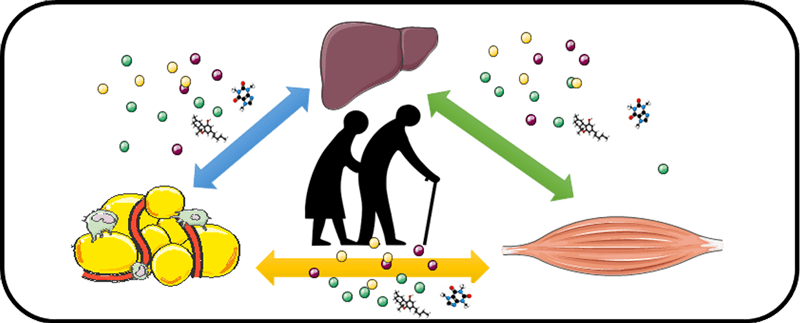
Le maintien de l’homéostasie énergétique aux cours des fluctuations environnementales est dû à une flexibilité métabolique de l’organisme. Dans ce contexte, de nombreuses modifications du métabolisme cellulaire / tissulaire sont soutenues par le métabolisme redox ainsi que par les interactions métaboliques intercellulaires et inter-organes qui sont fondamentales pour maintenir l’homéostasie énergétique des tissus et de l’organisme.
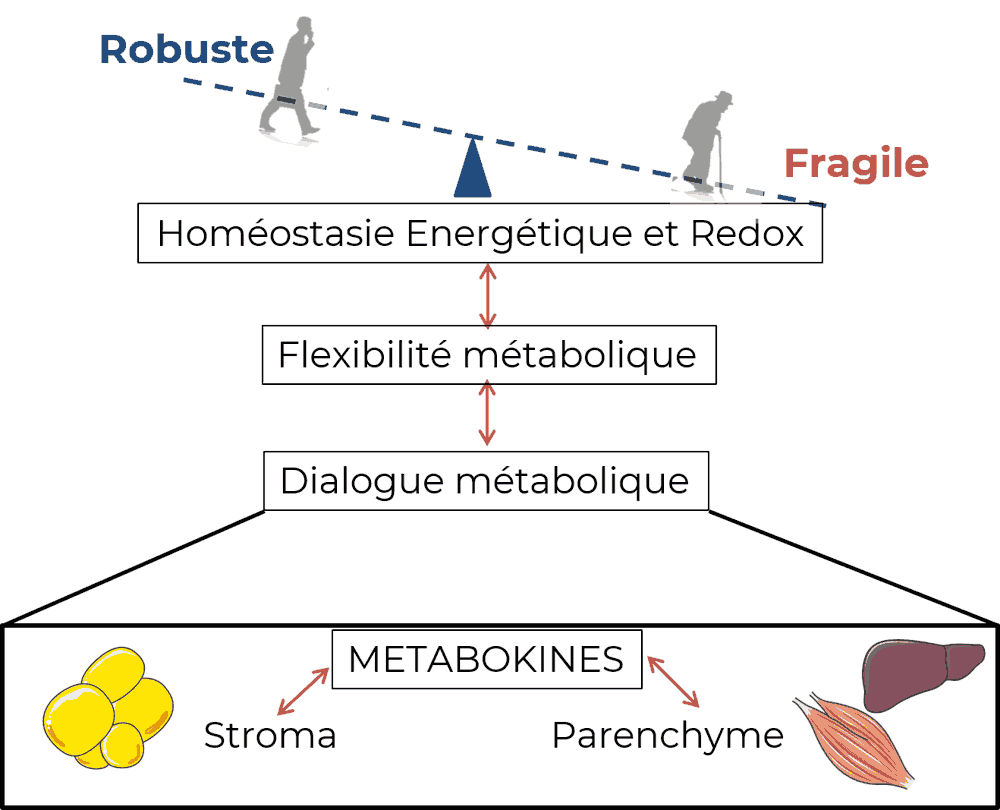
Nous avons émis l’hypothèse que la résilience métabolique (capacité cellulaire à faire face aux altérations métaboliques) permet à l’organisme vieillissant de maintenir les principales fonctions métaboliques (stockage, utilisation et libération d’énergie) nécessaires pour évoluer vers un vieillissement en bonne santé ou une dépendance en cas de perturbation.
Notre objectif est d’étudier le rôle et la régulation du dialogue métabolique local / systémique au sein d’un tissu (mésenchyme / parenchyme) et entre les tissus métaboliques (tissus adipeux / muscle / foie) en nous concentrant sur les modifications intracellulaires des voies métaboliques et l’état redox déclenchant des modifications majeures de sécrétion et de production cellulaire. Cela permettra d’identifier de nouveaux mécanismes qui contribuent, lorsqu’ils sont défectueux, à l’apparition ou à l’aggravation de maladies liées à l’âge (sarcopénie, maladies métaboliques) et qui pourraient représenter des cibles thérapeutiques d’intérêt.
Les axes de recherche
AXE 1
Métabokines et perte de fonction liée à l'âge
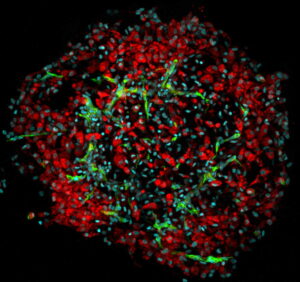 Les interactions métaboliques intercellulaires et interorganes sont fondamentales pour maintenir l’homéostasie énergétique des tissus et de l’organisme. Les effecteurs de ces interactions métaboliques comprennent à la fois des hormones / cytokines et des métabolites (regroupés sous le terme de «métabokines»), ces derniers pouvant agir comme des nutriments ou des molécules de signalisation.
Les interactions métaboliques intercellulaires et interorganes sont fondamentales pour maintenir l’homéostasie énergétique des tissus et de l’organisme. Les effecteurs de ces interactions métaboliques comprennent à la fois des hormones / cytokines et des métabolites (regroupés sous le terme de «métabokines»), ces derniers pouvant agir comme des nutriments ou des molécules de signalisation.
Avec l’âge, ces modifications du profil des «métabokines» pourraient interférer avec le dialogue entre les tissus métaboliques tels que les tissus adipeux, les muscles et le foie et par conséquent favoriser le déclin de la flexibilité métabolique au cours du vieillissement. Par conséquent, l’impact du vieillissement sur la distribution globale des flux de «métabokines» sera étudié.
Pour cela, nous développons de nouveaux modèles de vieillissement précoce ou accéléré (Nothobranchuis Furzeri, maladies génétiques, apport nutritionnel) associés à des approches de pointe (fluxomique, organ-on-chip) capables d’identifier et de cibler de nouvelles voies et des candidats thérapeutiques.
AXE 2
L'état redox, un nouveau déclencheur du vieillissement
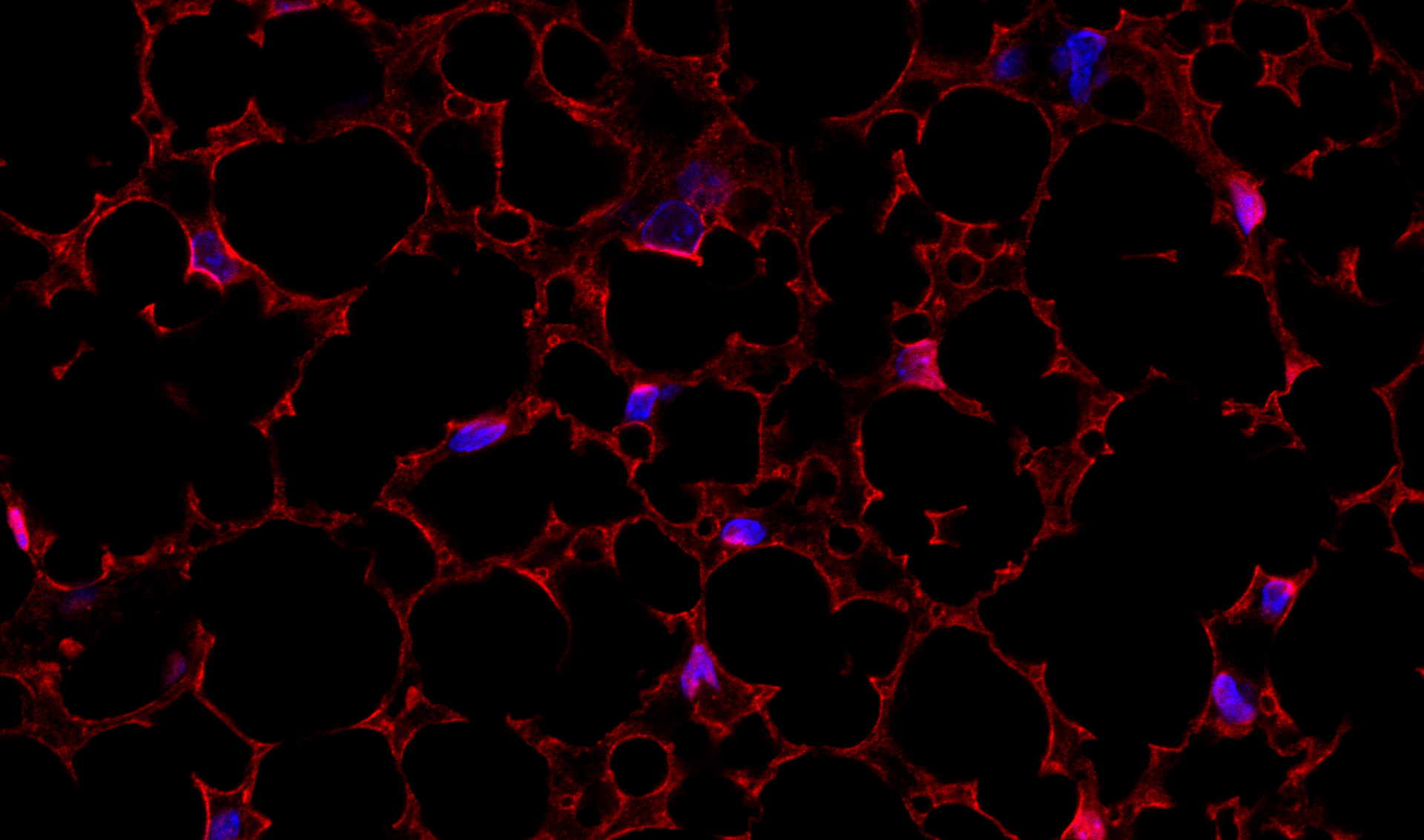 En utilisant des modèles animaux expérimentaux et des ressources humaines à jour, nous établissons le lien entre la perte des fonctions métaboliques liée à l’âge et l’état redox et étudions les causes et les conséquences des altérations de la flexibilité métabolique au cours du vieillissement des tissus métaboliques.
En utilisant des modèles animaux expérimentaux et des ressources humaines à jour, nous établissons le lien entre la perte des fonctions métaboliques liée à l’âge et l’état redox et étudions les causes et les conséquences des altérations de la flexibilité métabolique au cours du vieillissement des tissus métaboliques.
De nombreux aspects du métabolisme cellulaire / tissulaire sont déterminés par le métabolisme redox qui correspond à un réseau complexe de transfert d’électrons. Le maintien de l’homéostasie redox est d’une importance capitale pour les fonctions des cellules et des tissus et il a été démontré que l’état redox joue un rôle déterminant dans la réorganisation métabolique pendant le stress, grâce à la flexibilité métabolique.
En plus de soutenir l’homéostasie énergétique, l’état redox intervient aussi dans de nombreuses fonctions cellulaires, notamment la prolifération cellulaire, la différenciation, la sénescence ainsi que l’activité autocrine / paracrine / endocrinienne. Si le stress redox est bien connu pour être associé au vieillissement, Metabolink vise à comprendre et à cibler le réseau et la dynamique des réorganisations métaboliques et redox associées au vieillissement et aux pathologies associées à l’âge.
membres de l'équipe
Apeline, sarcopénie, vieillissement, adipokines, myokines, métabolisme


Annabelle BRU
Syndrome de Noonan, Sarcopénie, Inflammation, Macrophage, Viellissement, Sénescence

Métabolisme, adipocytes, métabolomique, fluxomique, traçage isotopique in vitro/in vivo, culture cellulaire en hypoxie, activité mitochondriale

Métabolisme, réseaux métaboliques, métabolomique, fluxomique

Exploration fonctionnelle in vivo, phénotypage métabolique, chirurgie

Anesthésie, réanimation, douleur

Métabolisme, réseaux métaboliques, métabolomique, fluxomique, modélisation métabolique

Foie, tissu adipeux, macrophages, métabolisme, inflammation, vieillissement

Apeline/APJ, obesité, adipokines, diabète, vieillissement

Publications
Morin E, Doumard E, Hartnell LM, Salegi Ansa B, Leduc-Gaudet JP, Quillien A, Nakhle J, Ethuin S, Goudounèche D, Payré B, Soldan V, Balor S, Mattout A, Rouquette J, Dubois L, Sengenès C, Planat V, Casteilla L, Yart A, Dray C, Aligon J, Ferrucci L, Duchesne É, Hussain SNA, Gouspillou G, Formentini L, Mourier A, Baris OR, Valet P, Parpex H, Monsarrat P, Vigneau M, Pradère JP.EMito-Metrix enables automated evaluation of mitochondrial morphology across species.Nat Metab. 2025 Oct 15. doi: 10.1038/s42255-025-01400-z.
Brodeau C, Joly C, Chekroun A, Nakhle J, Blase V, Espagnolle N, Dray C , Yart A, Planat V , Tertrais M, Fassy J, Guyonnet S, Lu WH, de Souto Barreto P, Teste O, Tremblay-Franco M, Tanner K, Cohen AA, Carriere A, Casteilla L, Ader I. Identification of Functional Cellular Markers Related to Human Health, Frailty and Chronological Age. Aging Cell. 2025 Sep;24(9):e70153. doi: 10.1111/acel.70153.
Montané R, Jeanson Y, Lagarde D, Khoury S, Porcher-Bibes L, Nakhle J, Sallese M, Parny M, Raymond-Letron I, Huard E, de Souza RA, Galinier A, Pellerin L, Sore AB, Pradère JP, Moro C, Casteilla L, Yart A, Dray C, Portais JC, Ader I, Carriere A. A brown adipose tissue activity impacts systemic lactate clearance in male mice. J Physiol. 2025 Sep 22. doi: 10.1113/JP288871.
Tremblay-Franco M, Canlet C, Carriere A, Nakhle J, Galinier A, Portais JC, Dray C, Wan-Hsuan P, Bertrand Michel J, Guyonnet S, Rolland Y, Delrieu J, de Souto Barreto P, Vellas B, Penicaud L, Casteilla L, Ader I. Integrative multi metabolomics to early predict cognitive decline among amyloid positive community-dwelling older adults. J Gerontol A Biol Sci Med Sci. 2024 79(5):glae077. doi: 10.1093/gerona/glae077
Farge T, Nakhle J, Lagarde D, Cognet G, Polley N, Castellano R, Nicolau M-L, Bosc C, Sabatier M, Sahal A, Saland E, Jeanson Y, Guiraud N, Boet E, Bergoglio C, Gotanègre M, Mouchel P-L, Stuani L, Larrue C, Moro C, Dray C, Colette Y, Raymond-Letron I, Ader I, Récher C, Sarry J-E, 3 Cabon F, Vergez F, and Carrière A. CD36 drives metastasis and relapse in acute myeloid leukemia. 2023. Cancer Res;83:2824 – 38
Pey V, Doumard E, Komorowski M, Rouget A, Delmas C, Vardon-Bounes F, Poette M, Ratineau V, Dray C, Ader I, Minville V. A locally optimised machine learning approach to early prognostication of long-term neurological outcomes after out-of-hospital cardiac arrest. Digit Health. 2024 Apr 15;10:20552076241234746. doi: 10.1177/20552076241234746
Kemoun P., Ader I., Planat-Benard V., Dray C., Fazilleau N., Monsarrat P., Cousin B., Paupert J., Ousset M., Lorsignol A., Raymond-Letron I., Vellas B., Valet P., Kirkwood T., Beard J., Pénicaud L., Casteilla L. A gerophysiology perspective on healthy ageing. Ageing Res Rev. 2022, 73:101537. Review
Ader I., Pénicaud L., Andrieu S., Beard J.R., Davezac N., Dray C., Fazilleau N., Gourdy P., Guyonnet S., Liblau R., Parini A., Payoux P., Rampon C., Raymond-Letron I., Rolland Y., De Souto Barreto P., Valet P., Vergnolle N., Sierra F., Vellas B., Casteilla L. Healthy Aging Biomarkers: The INSPIRE’s Contribution. J Frailty Aging. 2021,10(4):313-319
Bullich S., De Souto Barreto P., Dortignac A., He L., Dray C., Valet P., Guiard BP. Apelin controls emotional behavior in age- and metabolic state-dependent manner Psychoneuroendocrinology. 2022,140:105711
Paccoud R., Saint-Laurent C., Piccolo E., Tajan M., Dortignac A., Pereira O., Le Gonidec S., Baba I., Gélineau A., Askia H., Branchereau M., Charpentier J., Personnaz J., Branka S., Auriau J., Deleruyelle S., Canouil M., Beton N., Salles J.P., Tauber M., Weill J., Froguel P., Neel B.G., Araki T., Heymes C., Burcelin R., Castan I., Valet P., Dray C., Gautier E.L., Edouard T., Pradère J.P., Yart A.. SHP2 drives inflammation-triggered insulin resistance by reshaping tissue macrophage populations. Sci Transl Med. 2021;13(591):eabe2587
Lagarde D., Jeanson Y., Portais J.C., Galinier A., Ader I., Casteilla L, Carrière A. Lactate Fluxes and Plasticity of Adipose Tissues: A Redox Perspective. Front Physiol. 2021,12:689747. Review
Lagarde D., Jeanson Y., Barreau C., Moro C., Peyriga L., Cahoreau E., Guissard C., Arnaud E., Galinier A., Bouzier-Sore A.K., Pellerin L., Chouchani E.T,. Pénicaud L., Ader I., Portais J.C., Casteilla L., Carrière A. Lactate fluxes mediated by the monocarboxylate transporter-1 are key determinants of the metabolic activity of beige adipocytes. J Biol Chem. 2021, 296:100137
Stuani L., Sabatier M., Saland E., Cognet G., Poupin N., Bosc C., Castelli F.A., Gales L., Turtoi E., Montersino C., Farge T., Boet E., Broin N., Larrue C., Baran N., Cissé M.Y,. Conti M., Loric S., Kaoma T., Hucteau A., Zavoriti A., Sahal A., Mouchel P.L., Gotanègre M., Cassan C., Fernando L., Wang F., Hosseini M., Chu-Van E., Le Cam L., Carroll M., Selak M.A, Vey N., Castellano R., Fenaille F., Turtoi A., Cazals G., Bories P., Gibon Y., Nicolay B., Ronseaux S., Marszalek J.R., Takahashi K., DiNardo C.D., Konopleva M., Pancaldi V., Collette Y., Bellvert F., Jourdan F., Linares L.K., Récher C., Portais J.C., Sarry J.E. Mitochondrial metabolism supports resistance to IDH mutant inhibitors in acute myeloid leukemia. J.Exp Med. 2021, 218(5):e2020092
Tajan M., Hennequart M., Cheung E.C., Zani F., Hock A.K., Legrave N., Maddocks O.D.K., Ridgway RA, Athineos D., Suárez-Bonnet A., Ludwig R.L., Novellasdemunt L., Angelis N., Li V.S.W., Vlachogiannis G., Valeri N., Mainolfi N., Suri V., Friedman A., Manfredi M., Blyth K., Sansom O.J., Vousden K.H. Serine synthesis pathway inhibition cooperates with dietary serine and glycine limitation for cancer therapy Nat Commun. 2021,12(1):366
Millard U., Schmitt P., Kiefer J.A., Vorholt S., Heux S., Portais J.C. ScalaFlux: A scalable approach to quantify fluxes in metabolic subnetworks. PLoS Comput Biol. 2020,16(4):e1007799.
Vinel C., Lukjanenko I., Batut A., Deleyruelle S., Pradere J.P., Le Gonidec S., Dortignac A., N. Geoffre, Pereira O., S. Karaz, U. Lee, M. Camus, K. Chaoui, E. Mouisel, A. Bigot, V. Mouly, M. Vigneau, A. Pagano, A. Chopard, Pillard F., S. Guyonnet, M. Cesari, O. Schiltz, M. Pahor, J. Feige, B. Vellas, Valet P., DrayC. The exerkine apelin reverses age-associated sarcopenia. Nat. Med., 2018, 24: 1360-137
- I.Ader, Guyonnet S, Vellas B, Casteilla L, Bordeau C. Methods for predicting the health state of a subject from fibroblasts. Ep N°24306153.8
- I.Ader, Casteilla L, Tremblay-Franco M, Canlet C, Vellas B. Methods for predicting cognitive decline in a subject Ep N° 23306392.4
- I. Ader, J. Aligon, S. Cussat-blanc, L. Penicaud, P. Kemoun , D. Bernard, E. Doumard, P. Monsarrat, L. Casteilla. A method for determinig a physiological age of a subject. Ep N°22305353
- L. Mazeyrie, T. Edouard, C. Dray, J.P. Pradère, P. Valet, A.Yart : Use of Shp2 Inhibitors for inhibiting senescence Ep N° 22305331.1
- R. Paccoud, M. Tajan, P. Valet, C. Dray, J.P. Pradère, A. Yart : Use of Shp2 Inhibitors for the treatment of insulin resistance Ep N°18306558.0
- C. Dray, V. Minville, B. Frances, P. Valet: Method and pharmaceutical composition for the treatment of post-operative cognitive dysfunction. Ep N°16305170.9
- C. Dray, C. Knauf, O. Kunduzova, I. Castan-Laurell, P. Valet: Method dnd pharmaceutical composition for use in the treatment of dysfunction associated with aging. Ep N° 2 785 365
Financements



ANR JC
2025-2029: MIRAGE Restoring adipose tissue-skeletal muscle metabolic interactions to rejuvenate aging muscle
ANR
2021-2025: OPTISTEM Optimze MSC production.
2021-2025 LIVERSENES Liver senescence integrates the hallmark of aging.
2022-2025: ASCending Décryptage des réseaux métaboliques dans les ASCs en culture par un processus optimisé et contrôlé de production de cellules pharmaceutiques.
2022-2026: IRONAML53 Uncovering and targeting metabolic vulnerabilities of acute myeloid leukemia harboring TP53 mutations promoting Darwinian advantages in leukemic evolution and drug resistance.
2022-2027: RASORES Approches précliniques du traitement des patients atteints de RASopathie par une approche multiomique de leur physiopathologie à partir d’une cohorte de patients décrite et annotée de manière approfondie dans un registre européen dédié.
2023-2027: MESSAGE Etude des anomalies de la lignée myélomonocytaire dépendantes de SHP2 et contribution aux pathologies liées à l’âge
2024-2027: MetaOrgan Controlling metabolism to drive a fully functional standardized human beige adipose tissue organoid
PROJETS Région Midi-Pyrénées/FEDER
2015-2018: NIAGE Impact d’une alimentation à base d’insectes sur le vieillissement musculaire
2016-2017: TAMISE Vieillissement du macrophage du tissu adipeux blanc au cours de l’obésité
PROJETS Région Occitanie/FEDER
2019-2021: NURISENS Autotest urinaire connecté pour un suivi de la nutrition et de l’activité physique
2019-2021: IRISH Potentiel thérapeutique d’inhibiteurs de SHP2 dans le traitement de l’insuline-résistance
2019-2022: INSPIRE
2019-2022: MODELAGE Modélisation du vieillissement musculaire par des interventions nutritionnelles
2019-2022: BACTAGE Relation microbiote/sarcopenia au cours du vieillissement: impact d’un traitement au PDX
2019-2022: APELYM3D Analyse du rôle de l’apeline dans la restauration de la fonction lymphatique et du tissu adipeux par l’imagerie 3D.

























