Les équipements
RESTORE dispose d’un vaste parc instrumental mis à la disposition des scientifiques et géré par le CERT. Chacun de ces instruments profite également de l’expertise associée des ingénieurs et techniciens du laboratoire.
Par catégorie
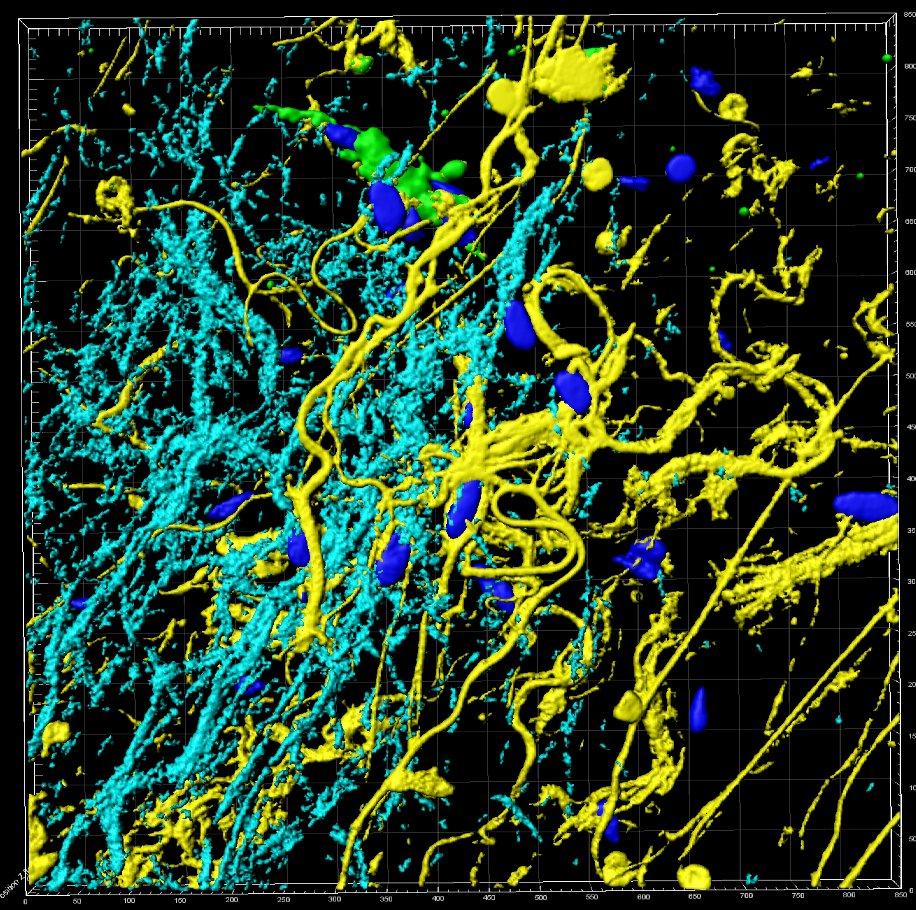
Imagerie 3D en profondeur
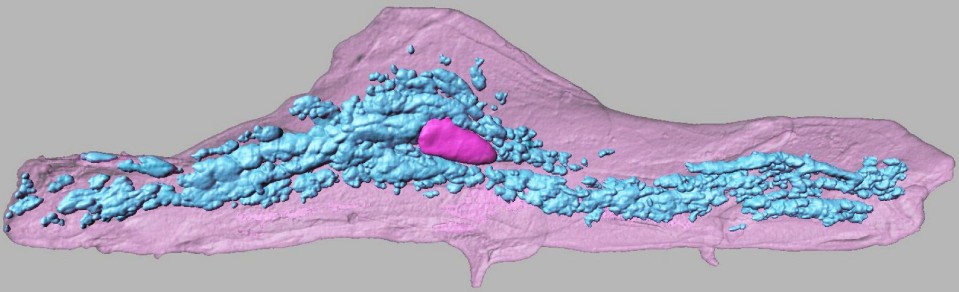
L’un des challenges en imagerie biologique est de visualiser en trois dimensions et en profondeur des structures biologiques et des organismes vivants. Le CERT dispose des instruments et de l’expertise permettant de réaliser ce type d’analyse. L’un d’entre eux, le SPIM, fruit des recherches du CERT et d’autres laboratoires toulousains, demeure un outil unique en plateforme.
Lightsheet Zeiss Z7

Descriptif du système
Le Z7 permet d’illuminer un plan entier de l’échantillon à l’aide d’une feuille de lumière en profondeur.
L’assemblage de ces acquisitions permet de reconstituer une image 3D de l’échantillon. La fluorescence émise par l’échantillon est détectée à 90° par rapport au plan d’illumination.
Spécifications :
Objectifs de détection:
5X Neofluar NA 0.16
20X Neofluar NA 1
Sources d’illumination:
laser 488nm
laser 515nm
laser 561nm
laser 638nm
Détecteur :
2 x Caméra PCO.Edge 4.2 monochrome (sCMOS ) 2048x 2048 pixel, 6.5µm taille pixel
Incubation:
Contrôle de la température et C02
Applications :
- Imagerie 3D en profondeur
- Imagerie in vivo
- Imagerie en multi-chanel, multi-plans en Z, multi-vues avec rotation de l’échantillon à 360°
MacroSPIM (indisponible)

Descriptif du système
Le MacroSPIM, macroscope basé sur une excitation à feuille de lumière, permet de visualiser après transparisation des tissus et des organes entiers par sectionnement optique rapide, en 3D et en profondeur.
Il offre des possibilités d’acquisition en multivues, ouvre de nouvelles perspectives dans l’observation biologique. Cet équipement unique basé sur un développement mené à Barcelone (IRB), est aujourd’hui, au sein du CERT, mis à la disposition de toute la communauté scientifique.
Spécifications :
Objectifs :
2x
5x
Zoom de 1X à 8X
Lasers :
405nm
488nm
561nm
642nm
Détecteurs :
2x Caméra ORCA Flash 4 (sCMOS) 2048×2048 pixels, 6.5µm taille pixel
Applications :
- Imagerie 3D en profondeur
- Imagerie de tissus et gros échantillons
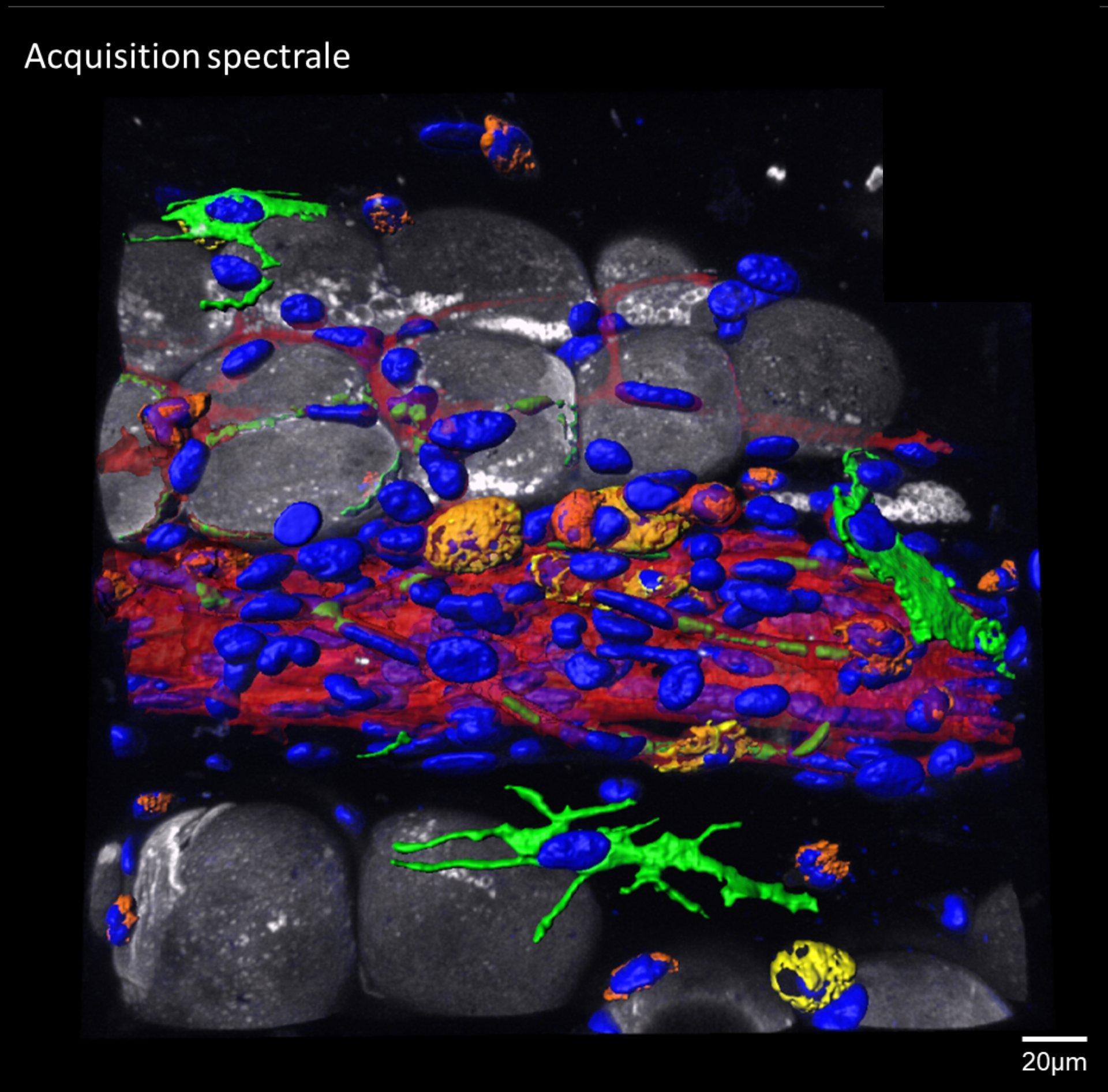
Imagerie spectrale
L’imagerie spectrale couplée au démixage linéaire permet de détecter et différencier des fluorophores dont les spectres se chevauchent. Il est aussi possible d’isoler l’autofluorescence de l’échantillon.
Confocal/Multiphoton Zeiss LSM880

Descriptif du système
Microscope confocal droit couplé à un laser multiphoton pour de l’imagerie sur des échantillons fixés (lame-lamelle) ou des échantillons « vivants » (explants, modèle animal).
Il permet également de l’imagerie sans marquage grâce à la détection du signal de génération de seconde (SHG) et troisième harmonique (THG).
Spécifications :
Statif :
AxioExaminer ( statif droit, distance maximale : 11cm)
Objectifs :
2.5X Fluar NA 0.12
10x Plan ApoChroma NA0.45
20x Plan ApoChroma NA 1
25x Plan Neofluar NA 0.8
40x ApoChroma NA 1.1
Détecteur :
– 2 PMTs latéraux
– 1 PMT détecteur spectral central GaAsP (32 détecteurs haute sensibilité)
– 1 détecteur NDD ( Détection 380-400 et 580-600)
Lasers:
– Argon 458, 488 et 514 nm
– DSSP 561nm
– Helium/Neon 633nm
– Ti/Sa Discovery ( Coherent) 690 – 1300 nm
Applications :
- Imagerie confocale et multiphoton
- Live imaging (explants et modèles animaux)
- Acquisition jusqu’à 10 canaux en simultané (8 GaAsP + 2 PMTs)
- Acquisition spectrale simultanée de 391 à 749 nm
- Imagerie Label Free : Génération de seconde et troisième harmonique ( SHG et THG) en simultanée
- Multi-positions et mosaïques
Imagerie en temps réel
Champ large AxioObserver Zeiss

Descriptif du système
La Vidéomicroscopie permet un suivi dynamique à long terme sur des échantillons « vivants » en 2D.
Nos systèmes possèdent des chambre d’incubation permettant des acquisitions de longues cinétiques en multi-position ou mosaïque, en fluorescence et transmission ( Champ Clair et Contraste de Phase)
Spécifications :
Objectifs :
5X Fluor NA 0.25
10X Achromat NA 0.25 PH1
10X Neofluar NA 0.3
20X Neofluar NA 0.5 PH2
40X Apochroma NA 0.95
63X Apochroma NA 1.4
Détecteur :
Caméra monochrome Axiocam 506 mono (CCD ZEISS) 2752 x 2208 pixel, 4.54µm taille pixel
Incubation:
Contrôle de la température et C02
Cubes filtres fluorescence :
DAPI
GFP
Yellow
DsRed
Cy5
Supports d’échantillons disponibles :
Insert plaque multi-puits
Insert universel
Insert 4 lames
Applications :
- Live imaging en 2D
- Multi-canaux
- Multi-position et mosaïques
Incucyte S3

Descriptif du système
L’incucyte S3 est un système d’imagerie et d’analyse automatisés permettant de suivre l’évolution des cellules dans un environnement thermorégulé.
Ce système permet un suivi jusqu’à plusieurs semaines et sur différentes plaques grâce à ses multiples emplacements disponibles.
Spécifications :
Objectifs:
4x
10x
20x
Canaux:
-Contraste de phase
-Fluorescence Vert ( Ex : 440-480nm, Em: 504-544nm)
-Fluorescence Rouge ( Ex : 565-605nm, Em: 625-705nm)
Incubation :
Temperature 37°C et 5% CO2
Supports d’échantillons disponibles :
6 emplacements plaque multi-puits
Modalités possibles:
– Standard
– Image Lock
– Scratch Wound
– Whole Well
– Dilution Cloning
– Chemotaxis
Applications :
- Live imaging en 2D
- Acquisition de court et long time-lapse ( jours, semaines)
- Multi-canaux
- Analyse quantitative du taux de prolifération cellulaire, migration et invasion.
Autres équipements
Champ large Eclipse Ti NIKON

Descriptif du système
Le Eclipse Ti NIKON permet des acquisitions d’échantillon en 2D sous diverses formats grâce à ses objectifs à longue distance de travail.
Ce système est idéal pour des acquisitions de marquages histologique et sur des lames de malassez grâce à sa caméra couleur.
Spécifications :
Objectifs :
2X Achromat NA 0.1
4X Plan Fluor NA 0.13 PHL
10X Plan Fluor NA 0.3 PH1
20X Plan Fluor NA 0.45 PH1
40X Plan Fluor NA 0.6 PH2
Détecteur :
Caméra couleur Nikon Ds Ri1 1280 x 1024 pixel, 6.45 µm taille pixel
Cubes filtres fluorescence :
DAPI
GFP
Cy3
Cy5
Supports d’échantillons disponibles :
Insert plaque multi-puits
Insert universel
Insert 4 lames
Applications :
- Multi-canaux
- Imagerie coloration ( B-Gal, bleu de Trypan, éosine)
MacroFluo

Descriptif du système
Ce système permet des acquisitions sur de large champs visuels et de grandes distances de travail, permettant ainsi la manipulation de gros échantillons.
Ce système est un bon choix pour examiner les effets d’un défaut génétique ou modification transgénique sur des modèles vivants, des boite de petri ou tissus.
Spécifications :
Objectifs :
0.5X Plan Apo
2X Plan Apo
5X Plan Apo
Détecteur :
Caméra Monochrome CoolSNAP HQ2 1392 x 1040 pixel, 6.45 µm taille pixel
Cubes filtres fluorescence :
DAPI
GFP
N3
FarRed
Applications :
- Imagerie animal (drosophile, zebrafish, souris) et gros échantillon ( tissus)
- Acquisition de boîte de pétri
- Cryostat Leica CM1950 – Coupes fines à congélation – Faculté de chirurgie dentaire
- Microtome HM340E – Coupes fines en paraffine – Faculté de chirurgie dentaire
- Vibroslice Campden 5100mz – Coupes épaisses en agarose – Incere
- Vibroslice Campden MA752 – Coupes épaisses en agarose – Faculté de chirurgie dentaire
Cytométrie en flux

Fortessa X20 - BD Biosciences
Le Fortessa X20 est équipé de 5 lasers : 488nm blue, 405nm violet, 355nm UV, 640nm red, 561nm yellow-green, pouvant lire 19 paramètres. Le Fortessa présent sur la plateforme est également équipé d’un passeur de plaques 96 puits. Le plateau est équipé des logiciels d’analyses DIVA, Flowlogic et Kaluza, utilisables sur place sous conditions de réservation.

MACSQuant - Miltenyi
Le MACSQuant est équipé de 3 lasers : 405nm, 488nm et 640nm, pouvant ainsi lire 10 paramètres. Ce cytomètre est également équipé d’un passeur de plaque, d’un module de marquage et de dilution automatique. Il permet de standardiser des expériences.
Tri cellulaire

ARIA Fusion - BD Biosciences
Le trieur présent sur le plateau, sous ambiance stérile, est un ARIA Fusion (BD Biosciences) équipé de 4 lasers : 561nm yellow-green, 407nm violet, 633nm red, 488nm blue, pouvant lire 18 paramètres.
Le trieur présent sur le plateau est équipé des accessoires suivant :
- Tri en 4 voies
- Tri en tubes de 1.5ml, 2ml, 5ml, 15ml
- Buse de 70µm, 85µm, 100µm
- Module de réfrigération en entrée et en sortie de tri.
Cytométrie en images

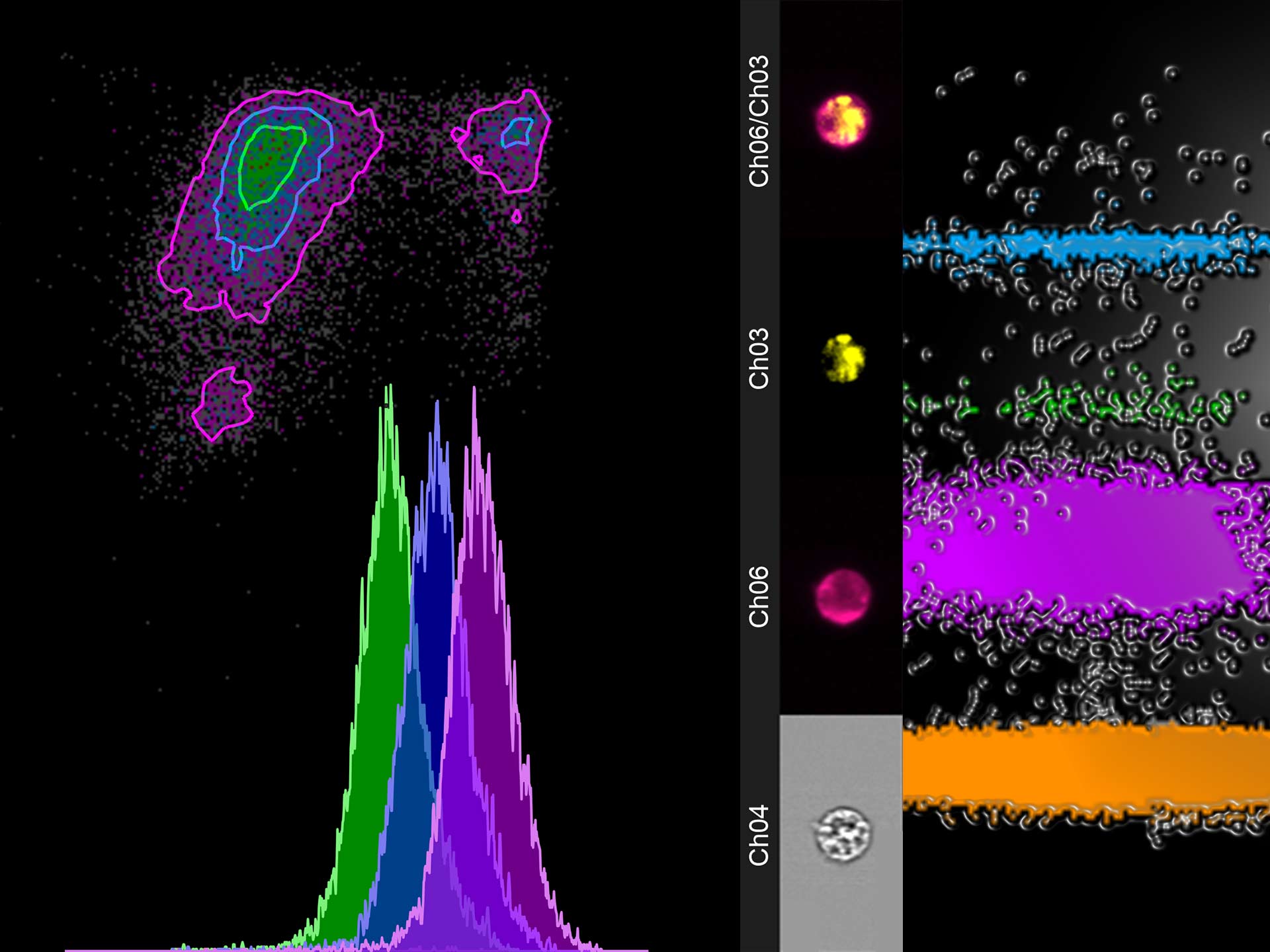
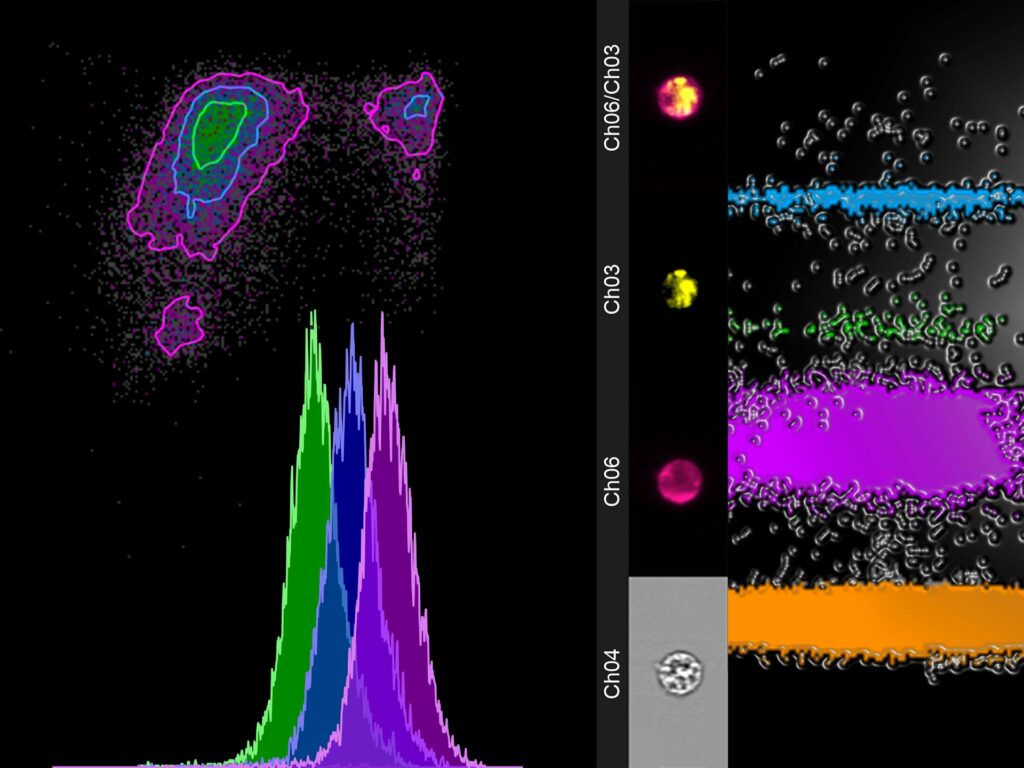
Image Stream X Mark 2 - Merck Luminex
Le plateau dispose d’un cytomètre en image : Image Stream X Mark II (Merck-Luminex). Cet appareil est équipé de 3 objectifs (20x, 40x et 60x, de 3 lasers (405nm, 488nm et 642nm) et d’une caméra et peut donc lire 6 paramètres simultanément.
Les fichiers d’images constitués de dizaines de milliers d’images de cellules peuvent être analysés de manière routinière en utilisant le logiciel IDEAS : analyse jusqu’à 500 paramètres morphométriques et photométriques pour chaque image de cellule utilisant des algorithmes brevetés. Le logiciel est présent sur le plateau est utilisable sous conditions de réservation.
Mécanobiologie-AFM

NanoWizard® II de JPK (Life Science Version)
Couplé à une microscope inversé à fluorescence Zeiss

Bioscope Catalyst de Bruker
Couplé à une microscope inversé à fluorescence Nikon.
- Couplages AFM-Photonique originaux
- Spectroscopie de force à l’air et en liquide avec pointes fonctionnalisées par chimie de surface.
- Topographie en mode contact, tapping et imagerie quantitative à l’air et en liquide
BioFab

Fabrication 3D : ZORTRAX INKSPIRE
- Printing Technology: UV LCD* – projecting a shape of a layer on the underside of the tank with liquid resin and curing the layer with a UV lamp
- Layer Thickness: 25, 50, 100 microns
- Pixel size: 50 microns (0.05 mm)
- Build Volume: 132 x 74 x 175 mm [2.9 x 5.2 x 6.9 in]
- Supported Formats: .cws, .zcodex, .sl1, .zip
- Operating Temperature: 20 – 30˚ C
- Software Bundle: Z-SUITE 2®
- Supported File Types: .stl, .obj, .dxf, .3mf, .zcodex
Lithographie 2D

Machine de lithographie douce Gesim (Micro-Contact Printing – µCP)
Soft UV-NIL (Encrage, Séchage, Dépôt de molécules, Insolation UV)

Plasma oxygene micro-ondes DIENER Pico & étuve MEMMERT

Microscope droit avec champ sombre

Spin coater LAURELL WS-650-SZ
Culture biologique

2 PSM avec filtre à charbon pour solvants

2 Incubateurs et 1 réacteur
Logiciels de traitement et d’analyse
Logiciels de traitement et d’analyse de données biologiques
|
Spécifications |
Applications |
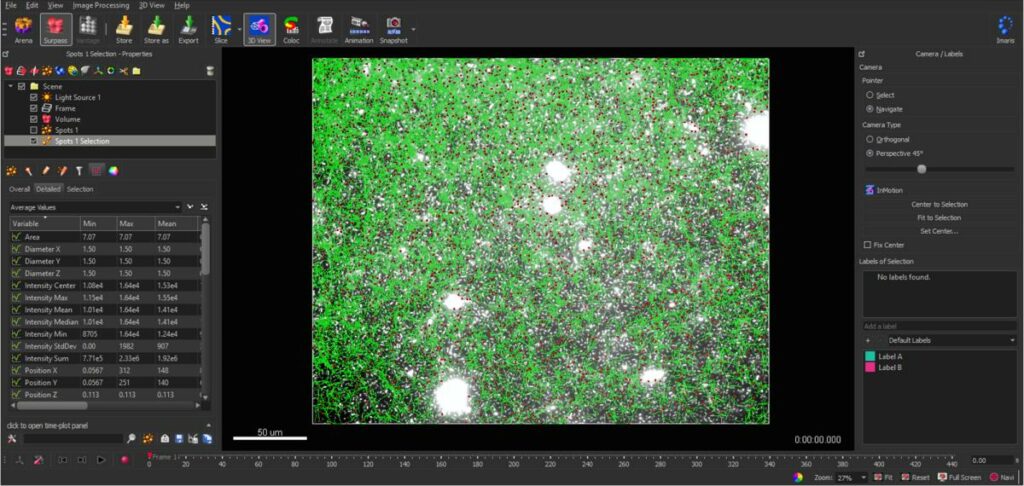
| 3 licences Imaris (Bitplane) | 3D & 4D modeling, 2D & 3D tracking |
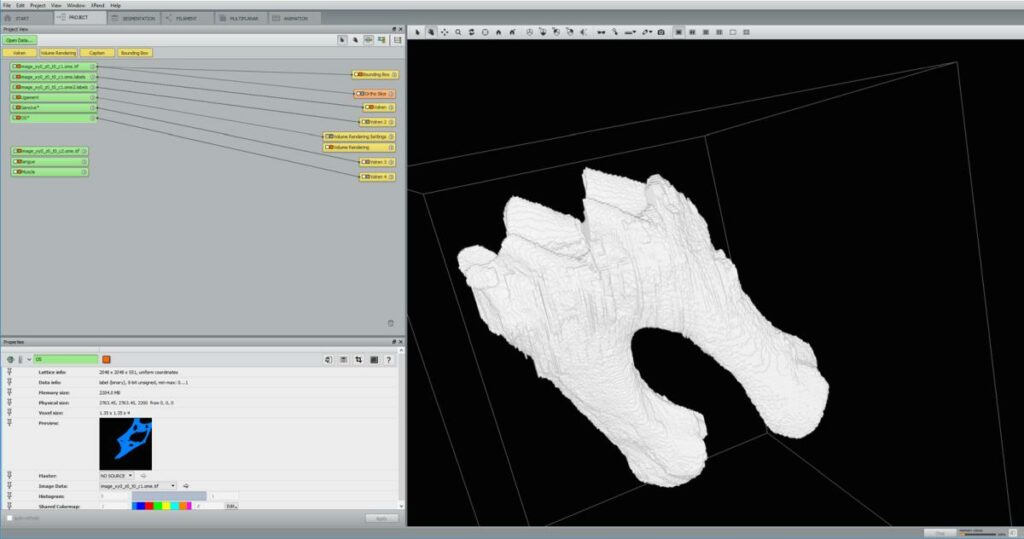
| 2 licences Amira (ThermoFisher) | 3D modeling, 3D & 4D image processing |
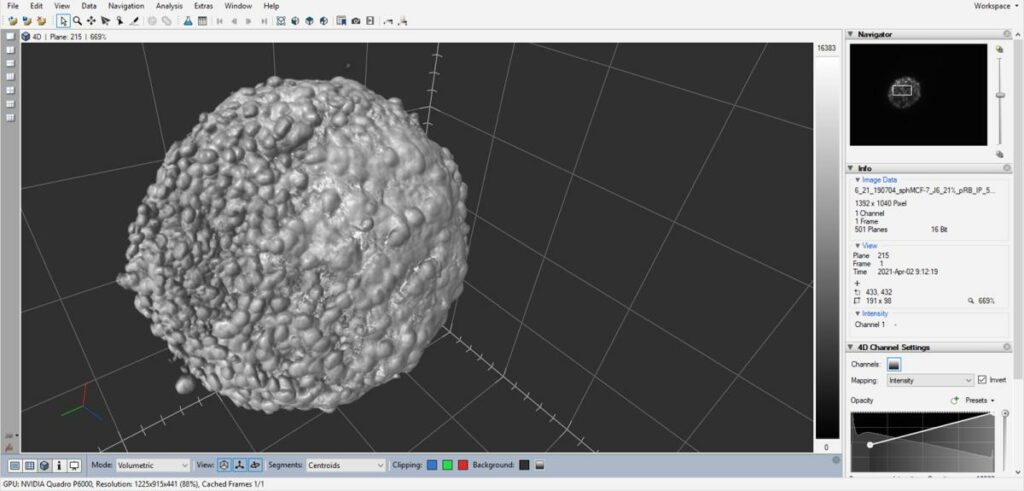
| 1 licence Vision 4D (Arivis) | 3D & 4D modeling, pixel & object classification |
| Serveur de licences Matlab (Mathworks) | Pixel & Object classification, workflow & automatic image processing, GUI implementation, database implementation |
| 3 licences NIS elements (Nikon) | 3D & 4D modeling, 2D & 3D tracking, Volume analysis, High content analysis |
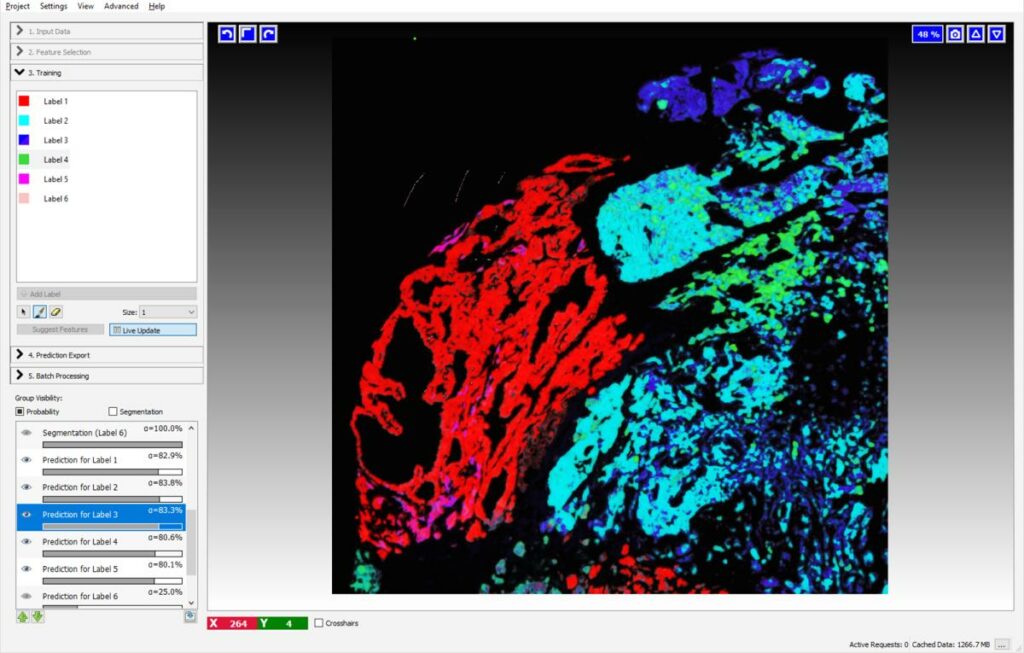
| Logiciels open-source Ilastik | Pixel & Object classification |
| Logiciels open-source Fiji | 2D, 3D & 4D image processing, Pixel & Object classification, 2D & 3D tracking, automatic image processing |
| Logiciel open-source Python | Pixel & Object classification, GUI implementation, database implementation |
| Licences Graphpad Prism | Statistical analysis of biological data |
| 3 licences Flowlogic | Flow Cytometry analysis |
| 5 licences Kaluza | Flow Cytometry analysis |
| 1 licence INSPIRE | Imaging Flow Cytometry analysis |
Logiciels d’analyse High Content Screening
Spécifications
- Une licence HCS Studio (ThermoFisher)
- 2 licences Harmony (Operetta)
- Système d’exploitation Windows 7 (64 bits)
Applications
- Real time acquisition and visualization of 2D, 3D et 4D images
- Automated high content analysis (Apoptosis, Cell cycle, cell proliferation, Cell viability, Neurite, outgrowth, protein synthesis)
- Visual and quantitative analysis of 2D, 3D and 4D cell models
Stations d’analyse

2 stations d’analyse Dell Precision T7910
Spécifications
- Processeur Intel Xeon CPU E5-2680 V4
- Carte graphique NVIDIA Quadro K6000 12GoApplications
- 256 Go de RAM
- Système d’exploitation Windows 10 (64 bits)
Applications
- Modélisation, visualisation d’images
- Analyse d’images
- Traitement d’images
- Calculs GPU & CPU
Training on qPCR instruments
Setting up an experimental protocol
Analysis and interpretation of results
Use of a 384-well plate dispenser
CONTACT
Pour toutes demandes, le personnel du CERT :
- assure le conseil dans l’élaboration des panels multi-couleurs,
- assure la formation des utilisateurs,
- assiste les utilisateurs dans l’analyse et l’interprétation de leurs résultats,
- accompagne les utilisateurs dans la mise en place de projet de recherche et développement, sous forme de collaboration.